Paris, France | AFP | vendredi 05/10/2018 - Un chercheur a affirmé avoir retrouvé des "impuretés" dans la nouvelle formule du Levothyrox, mais le CNRS, son employeur, a estimé vendredi qu'il n'avait "pas respecté la déontologie scientifique indispensable pour valider toute recherche".
Ce chercheur toulousain, Jean-Christophe Garrigues, a affirmé mercredi au site Médiacités avoir décelé des "éléments impurs" en analysant ce médicament, accusé par certains patients de provoquer des effets secondaires.
"Ce pic d'impureté alerterait le moindre scientifique", a-t-il assuré, sans nommer les substances selon lui en cause. Ses analyses ont été réalisées pour l'association de patients AFMT, en pointe dans la lutte contre le nouveau Levothyrox.
"En tant qu'employeur, le CNRS considère que l'agent n'a pas respecté la déontologie scientifique indispensable pour valider toute recherche", a réagi le CNRS dans un communiqué au ton inhabituellement vif.
"Les résultats annoncés par Jean-Christophe Garrigues, ingénieur de recherche au CNRS, n'ayant pas été validés par le processus d'évaluation par les pairs propre à la communauté scientifique, le CNRS considère qu'ils ne constituent pas en l'état actuel des faits scientifiques", a ajouté l'organisme de recherche.
Bien que le chercheur ait utilisé son équipement pour les réaliser, ces mesures "ne sont liées en aucune façon à une quelconque activité de recherche de son équipe ou du laboratoire", a poursuivi le CNRS, qui dit n'en avoir pas été informé.
Pour toutes ces raisons, "le CNRS et l'université Toulouse III Paul-Sabatier ont demandé l'annulation d'une conférence de presse" prévue vendredi matin dans leurs locaux par l'AFMT, à laquelle aurait dû participer M. Garrigues.
"Le CNRS et l'université Paul-Sabatier s'engagent à encourager leurs laboratoires compétents dans le domaine à travailler dans l'élucidation des questions soulevées par lesdits résultats", a conclu le CNRS.
De son côté, l'Agence du médicament ANSM a rappelé que "l'ensemble des contrôles réalisés dans (ses) laboratoires ont confirmé la bonne qualité de la nouvelle formule du Levothyrox".
Le laboratoire Merck, qui fabrique ce médicament, a lui dénoncé des "allégations sensationnalistes et sans preuve", en rappelant que de précédentes affirmations de l'AFMT sur la composition du médicament avaient déjà été "démenties par (...) les autorités sanitaires".
Enfin, Merck a démenti une hypothèse émise par Médiacités, selon lequel le labo aurait pu modifier "en catimini" la composition du nouveau Levothyrox depuis sa mise sur le marché l'an dernier.
Le site, dont Médiapart est un des actionnaires, avance que le labo aurait pu "limiter la présence d'éléments impurs" après les premières plaintes liées à la nouvelle formule.
"Il n'y a pas de +nouvelle-nouvelle formule+. Nous condamnons fermement toute allégation dans ce sens", a assuré le laboratoire.
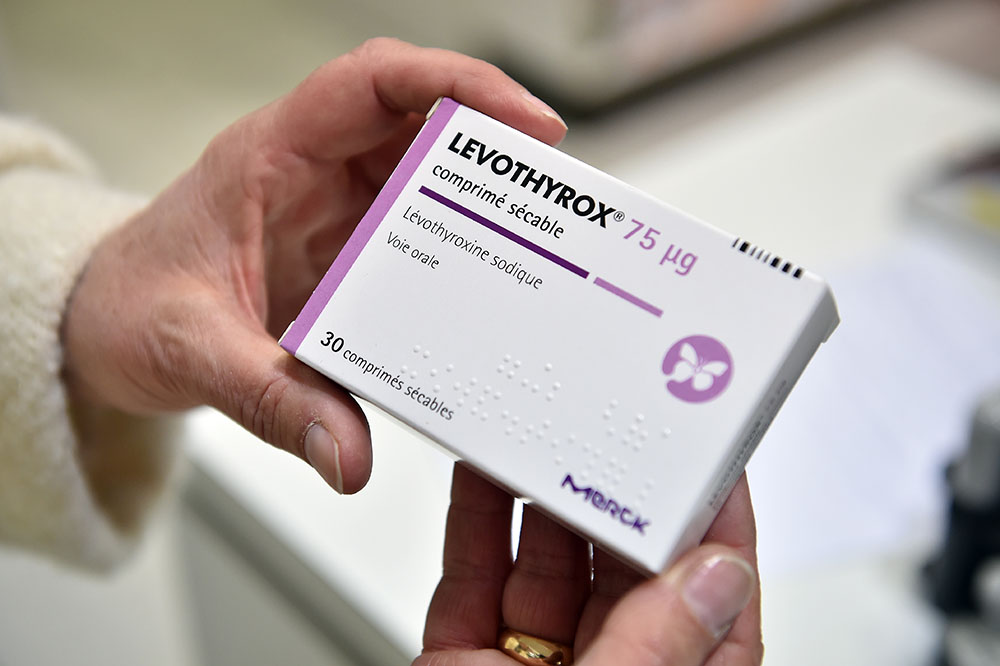
Mise sur le marché au printemps 2017, à la demande de l'ANSM, la nouvelle formule de ce médicament pour la thyroïde est accusée par des patients de provoquer une vague d'effets secondaires (fatigue, maux de tête, insomnies, vertiges, etc...).
Selon des chiffres officiels, quelque 31.000 patients (sur un total de 2,2 millions) se sont plaints d'effets indésirables.
L'affaire fait l'objet de plusieurs procédures en justice.
Ce chercheur toulousain, Jean-Christophe Garrigues, a affirmé mercredi au site Médiacités avoir décelé des "éléments impurs" en analysant ce médicament, accusé par certains patients de provoquer des effets secondaires.
"Ce pic d'impureté alerterait le moindre scientifique", a-t-il assuré, sans nommer les substances selon lui en cause. Ses analyses ont été réalisées pour l'association de patients AFMT, en pointe dans la lutte contre le nouveau Levothyrox.
"En tant qu'employeur, le CNRS considère que l'agent n'a pas respecté la déontologie scientifique indispensable pour valider toute recherche", a réagi le CNRS dans un communiqué au ton inhabituellement vif.
"Les résultats annoncés par Jean-Christophe Garrigues, ingénieur de recherche au CNRS, n'ayant pas été validés par le processus d'évaluation par les pairs propre à la communauté scientifique, le CNRS considère qu'ils ne constituent pas en l'état actuel des faits scientifiques", a ajouté l'organisme de recherche.
Bien que le chercheur ait utilisé son équipement pour les réaliser, ces mesures "ne sont liées en aucune façon à une quelconque activité de recherche de son équipe ou du laboratoire", a poursuivi le CNRS, qui dit n'en avoir pas été informé.
Pour toutes ces raisons, "le CNRS et l'université Toulouse III Paul-Sabatier ont demandé l'annulation d'une conférence de presse" prévue vendredi matin dans leurs locaux par l'AFMT, à laquelle aurait dû participer M. Garrigues.
"Le CNRS et l'université Paul-Sabatier s'engagent à encourager leurs laboratoires compétents dans le domaine à travailler dans l'élucidation des questions soulevées par lesdits résultats", a conclu le CNRS.
De son côté, l'Agence du médicament ANSM a rappelé que "l'ensemble des contrôles réalisés dans (ses) laboratoires ont confirmé la bonne qualité de la nouvelle formule du Levothyrox".
Le laboratoire Merck, qui fabrique ce médicament, a lui dénoncé des "allégations sensationnalistes et sans preuve", en rappelant que de précédentes affirmations de l'AFMT sur la composition du médicament avaient déjà été "démenties par (...) les autorités sanitaires".
Enfin, Merck a démenti une hypothèse émise par Médiacités, selon lequel le labo aurait pu modifier "en catimini" la composition du nouveau Levothyrox depuis sa mise sur le marché l'an dernier.
Le site, dont Médiapart est un des actionnaires, avance que le labo aurait pu "limiter la présence d'éléments impurs" après les premières plaintes liées à la nouvelle formule.
"Il n'y a pas de +nouvelle-nouvelle formule+. Nous condamnons fermement toute allégation dans ce sens", a assuré le laboratoire.
Mise sur le marché au printemps 2017, à la demande de l'ANSM, la nouvelle formule de ce médicament pour la thyroïde est accusée par des patients de provoquer une vague d'effets secondaires (fatigue, maux de tête, insomnies, vertiges, etc...).
Selon des chiffres officiels, quelque 31.000 patients (sur un total de 2,2 millions) se sont plaints d'effets indésirables.
L'affaire fait l'objet de plusieurs procédures en justice.